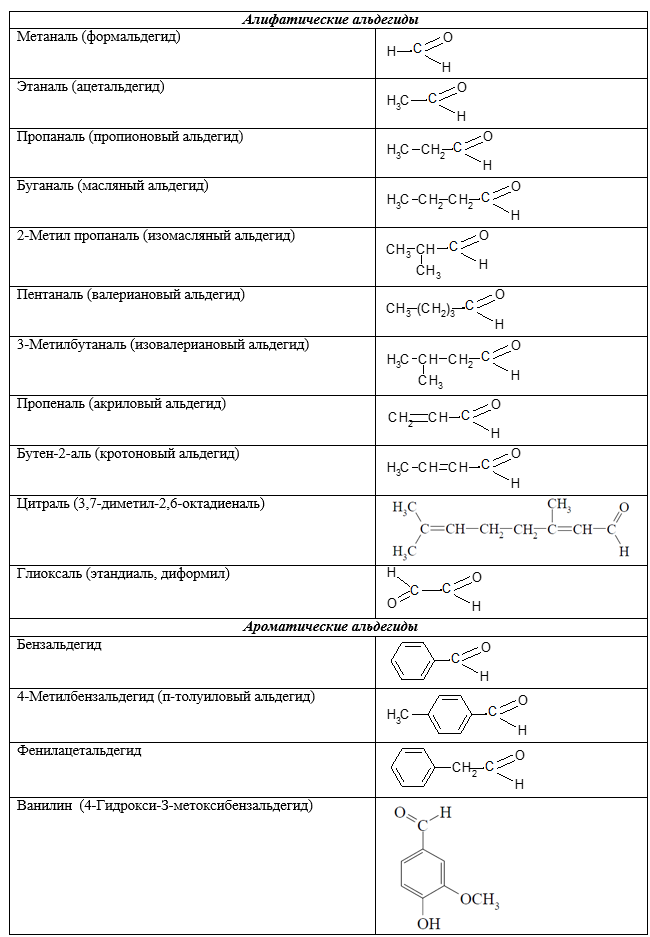
Формулы альдегидов
Формулы альдегидов
- Особенности номенклатуры
- Реакционная способность и реакционные центры
Альдегидами называются органические карбонильные соединения, которые имеют важнейшую группу С=О. Группа атомов С=O называется карбонильной группой или карбонилом. Далее эта группа соединяется с углеводородом и водородом, образуя строение
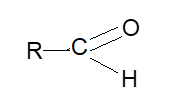
Их можно рассматривать как продукты окисления спиртов. Так, например, самый простой альдегид добывают окислением метилового спирта оксидом купрума(ll):
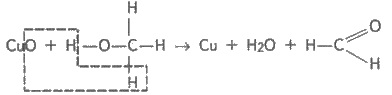
Если берется за основу особенности строения радикалов углеводорода, альдегиды делятся на:
- насыщенные алифатические;
- ненасыщенные алифатические;
- ароматические.
Особенности номенклатуры
Чтобы понять особенности формирования названий альдегидов, необходимо найти в международной номенклатуре название подобного алкана, с соответствующим набором углеродных атомов и добавить окончание –аль.
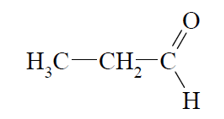
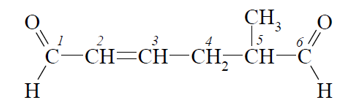
Чтобы рассмотреть правило подробнее, проделайте приведенный алгоритм:
- для обозначения определите цепь атомов углерода, которая будет самая длинная и включает альдегидную группу;
- сделайте нумерацию атомов, первым будет атом упомянутой альдегидной группы;
- найдите соответствующее название по принципу обозначения углеводородов;
- добавьте упомянутое окончание –аль.
Если мы обнаруживаем 3, 4 и т.д. альдегидные группы, то, соответственно названия будут связаны с этим. В результате получаем –трикарбальдегид, -тетракарбальдегид и т.д.
Если мы имеем боковую цепь или группа не является старшей, то номенклатура будет отмечена префиксом формил-.
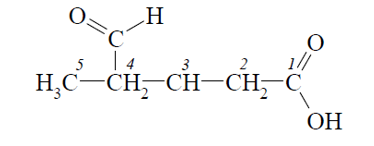
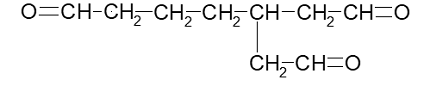
Цеклические альдегиды могут иметь непосредственную связь с атомом углерода, в этом случае используется окончание – карбальдегид.
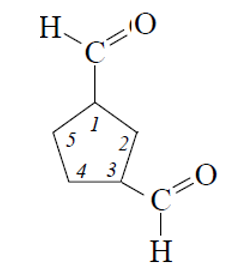
Существуют также альдегиды, которые имеют свои устойчивые названия. И данные названия, как правило, походят от кислот.
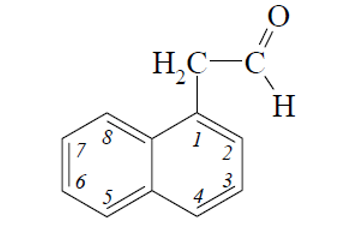
Реакционная способность и реакционные центры
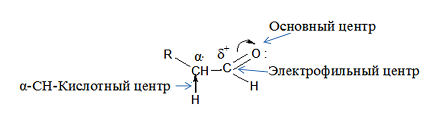
Реакционные центры в молекулах:
- связь С – Н разрывающаяся в процессе окисления;
- насыщенные и ароматические радикалы, которые подвергаются атаке электрофильными или нуклеофильными реагентами;
- а- СН- кислотный центр и индуктивный эффект. Благодаря ему происходит большая часть реакций (например, конденсация);
- электрофильный центр, который обеспечивает реакции присоединения;
- основной центр (с неподеленной электронной парой), который обеспечивает кислотный катализ в реакциях енолизации и присоединения.
На реакционную способность влияют многие факторы. И одним из них является полярность. Ведь нуклеофильная частица лучше атакует больший заряд +. Именно поэтому акцепторные заместители, которые перетягивают электроны, увеличивают способность карбонильной группы к реагированию. А донорные – снижают.
Мезомерный эффект в ароматических альдегидах снижает частичный положительный заряд. Именно поэтому данные альдегиды проявляют меньший эффект по сравнению с алифатическими альдегидами.
Реакционная способность также уменьшена у объемных радикалов. Это называется стерическим фактором. То есть таким фактором, который отслеживает взаимную ориентацию частиц, вступающих в реакцию, в случае их столкновений для обеспечения реакции. Суть его заключается в затрудненном подходе нуклеофилов к карбонильному углеродному атому.
